化学便覧を読むと『水の誘電率』『トルエンの誘電率』『固体の誘電率』など、様々な誘電率が紹介されています。
化学には沸点やpKaなど化学物質の性質を示す様々なパラメーターがありますが、誘電率というのは少し聞き慣れないかもしれません。
しかし、誘電率は化学物質の性質を表す重要なキーワードの一つです。
この記事では少しマイナーですが、でも重要な物性である誘電率についてざっくりと解説します。
誘電率とは?
誘電率は分子の静電相互作用を表す重要なパラメーターです。
誘電率とはその名前からイメージする通り、『電気の通りやすさ』を表す値です。
誘電率が高いとは電気を通しやすく、誘電率が低いとは電気を通しにくいことを意味します。
極性との関係
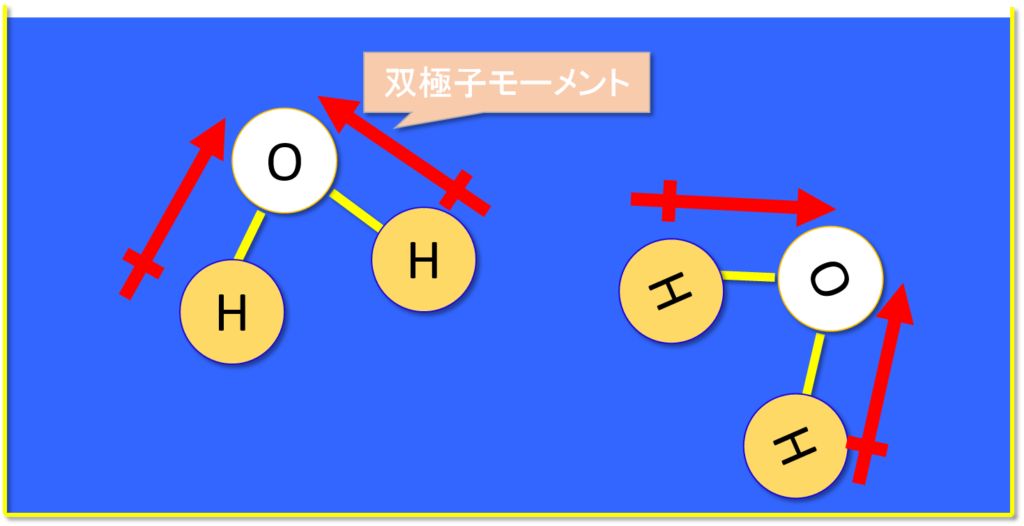
誘電率の大きさは極性の大きさに関係しています。
単純なアルキル鎖のみから構成されるヘキサンの誘電率(比誘電率)は1.9しかありませんが、エタノールは24.3もあり、実に13倍近くあります。
エタノールには電気陰性度の高い酸素Oが入っているためです。
加えて、水(H2O)は“水素結合”することで有名ですが、水素結合するほど極性が高いので誘電率も高く78.3(25℃)もあります。
基本的に化学構造の中に酸素Oや窒素Nが入っているような化合物は誘電率が高いです。
つまり極性が高いです。
電荷の偏りがある、すなわち『双極子モーメント』がある化学物質は誘電率・極性が高いと言えます。
逆にヘキサンやベンゼンのような炭素Cと水素Hのみから構成されるような分子は極性が小さく誘電率が小さいです。
そのため炭化水素の誘電率は小さいのが特徴です。
その他誘電率を決める要素
極性以外の影響
誘電率と極性の関係を述べましたが、誘電率には実は他の要素も関係してきます。
電離(電解質)
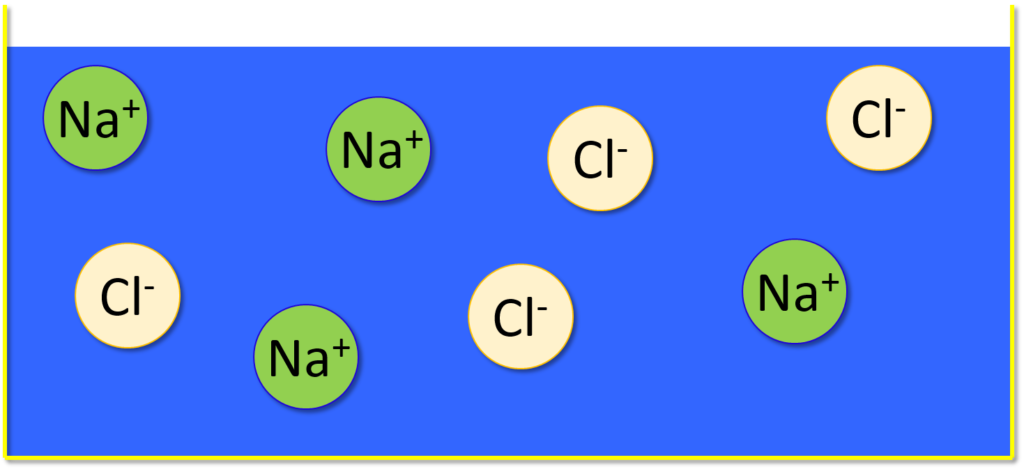
誘電率は物質の極性以外にも影響されます。
例えば、『電離』も重要な要素です。
実を言えば、水があれほど誘電率が高いのは極性が高いということの他に『電離する』という性質にも大きく影響されています。
カチオン(+)やアニオン(-)といった電荷を持った分子があると電気は流れやすくなります。
それは電場を掛けた時にカチオンやアニオンが電場の力により動くためです。
水は知ってのとおり、H+とOH–に電離しますので、電荷を持つ分子が液体中に存在しますので、誘電率が大きくなります。
ちなみに水に塩化ナトリウム(NaCl:食塩)を溶かすと誘電率が上がります。
理由は、塩化ナトリウムは水中で完全に電離してNa+とCl–になるためです。
溶けたNaClの濃度に応じて(比例はしない)、誘電率が大きくなります。
自由電子
 自由電子についてはあくまで『固体』に関係する話になります。
自由電子についてはあくまで『固体』に関係する話になります。
液体のイメージが強い方は、「固体なのに誘電率?」と思うかもしれませんが、電気を通すことができるかどうかが重要です。なので固体にも誘電率は当然あります。
金属は結晶内を自由に動き回る『自由電子』が存在することは高校化学で習ったと思います。
その電子は当然のことながら『マイナス』の電荷を帯びていますので、電場を掛けると陽極に移動します。
これはすなわち電気が流れていることを意味しますので、自由電子が多ければ多い方が誘電率は大きくなります。
誘電率の活用場面
溶解するかの予測
溶解性の推測
極性を表すパラメーターとして誘電率を参考にできます。
つまり誘電率が大きい分子を見て『極性が高いんだな。塩を溶解させそうだな。』とか『親水性の物質と混和しそうだ。』などの重要な推測を行うことができます。
『極性』というのは実は曖昧な概念なので、誘電率という数値化されたパラメーターは非常に参考になります。
静電相互作用の強さ
極性が高い場合、分子間の静電相互作用が大きい傾向にあります。
そのため誘電率が高い液体を見たとき、『沸点が高いのかな?』などの予想を立てることが出来ます。
その他に、『励起分子のエネルギー移動のしやすさ』も誘電率が参考になります。
光を吸収して励起状態になった水中の分子というのは、様々な要因でエネルギーを失いますが、その一つに『誘電率の高い溶媒との相互作用』があります。
励起状態にある不安定な分子が、周囲の高極性分子との間で安定化されることが原因です。
その結果、例えば『蛍光』は長波長シフト(低エネルギー化)します。
まとめ
誘電率は極性に関係する重要なパラメーターです。
溶解性などを予想するときに活用しましょう。
『誘電率が高い = 極性が高い』という関係から分子間の静電相互作用についても予想することが出来ます。